国家药监局】19批次药品(11批饮片)不合格,诊所从药材市场
6月20日, 国家药监局关于10批次药品不符合规定的通告(2022年第27号)
经福建省食品药品质量检验研究院等8家药品检验机构检验,标示为广西金嗓子药业股份有限公司等9家企业生产的小儿感冒颗粒等10批次药品不符合规定。现将相关情况通告如下:
一、经黑龙江省药品检验研究院检验,标示为福元药业有限公司生产的1批次阿达帕林凝胶不符合规定,不符合规定项目为pH值。
经云南省食品药品监督检验研究院检验,标示为荣康集团广西康世缘制药有限公司生产的1批次川贝止咳糖浆不符合规定,不符合规定项目为装量。经广西壮族自治区食品药品检验所检验,标示为江西山高制药有限公司生产的1批次冠脉宁胶囊不符合规定,不符合规定项目为鉴别;标示为山东昊福药业集团制药有限公司生产的1批次冠脉宁片(素片)不符合规定,不符合规定项目为重量差异。
经福建省食品药品质量检验研究院检验,标示为广西金嗓子药业股份有限公司生产的2批次小儿感冒颗粒不符合规定,不符合规定项目为鉴别。
经湖南省药品检验检测研究院检验,标示为四川逢春制药有限公司生产的1批次玄麦甘桔颗粒不符合规定,不符合规定项目为含量测定。
经青海省药品检验检测院检验,标示为西藏甘露藏药股份有限公司生产的1批次智托洁白丸不符合规定,不符合规定项目为性状、重量差异。
经四川省药品检验研究院(四川省医疗器械检测中心)检验,标示为*****堂中药饮片有限公司生产的1批次川牛膝不符合规定,不符合规定项目为性状。
经甘肃省药品检验研究院检验,标示为北海能信中药有限责任公司生产的1批次茜草不符合规定,不符合规定项目为性状、鉴别。
二、 对上述不符合规定药品,药品监督管理部门已要求相关企业和单位采取暂停销售使用、召回等风险控制措施,对不符合规定原因开展调查并切实进行整改。
三、 国家药品监督管理局要求相关省级药品监督管理部门依据《中华人民共和国药品管理法》,组织对上述企业和单位存在的涉嫌违法行为立案调查,并按规定公开查处结果。
附件:1.10批次不符合规定药品名单
2.不符合规定项目的小知识
附件:1.10批次不符合规定药品名单
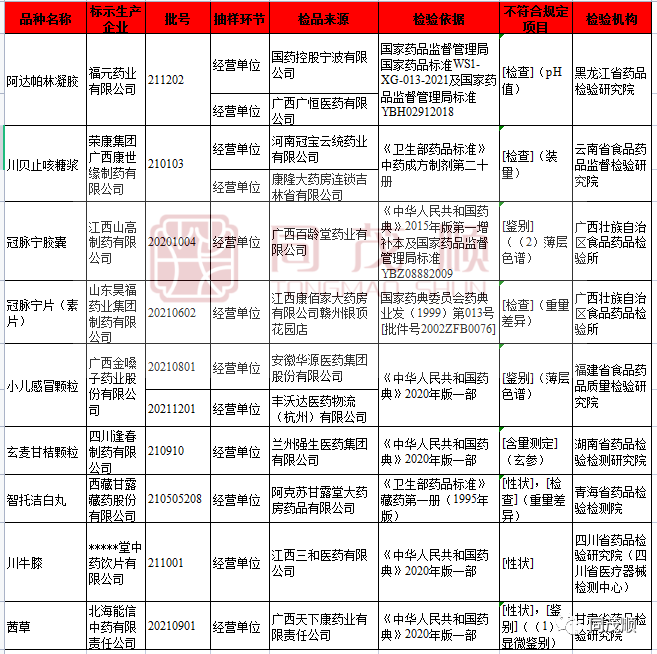
一、pH值是氢离子浓度指数,作为酸碱程度的衡量指标。
二、装量系反映药品重量或容量的指标,适用于固体、半固体、液体制剂,规定应按最低装量检查法进行检查,不符合规定会导致临床给药剂量不足。
三、鉴别项主要用于区分药品特性,其手段包括显微鉴别、光谱鉴别等,薄层色谱法是常用的鉴别方法。
四、重量差异系反映药物均匀性的指标,是保证准确给药的重要参数之一。
五、含量测定系指用规定的试验方法测定原料及制剂中有效成分的含量,一般可采用化学、仪器或生物测定方法。
六、性状项下记载外观、臭、味、溶解度以及物理常数等,在一定程度上反映药品的质量特性。中药饮片性状项不符合规定,可能涉及药材种属偏差、炮制工艺有瑕疵、储存不当等情形。
▍6月20日,重庆市药品监督管理局关于9批次药品不符合规定的通告
为加强药品质量监督管理,规范市场秩序,保障公众用药安全,我局组织局属检查局和各区县药品监管部门开展药品抽检。经重庆市食品药品检验检测研究院等检验机构检验,标示为河南尚华堂药业股份有限公司等企业生产的9批次药品不符合规定。
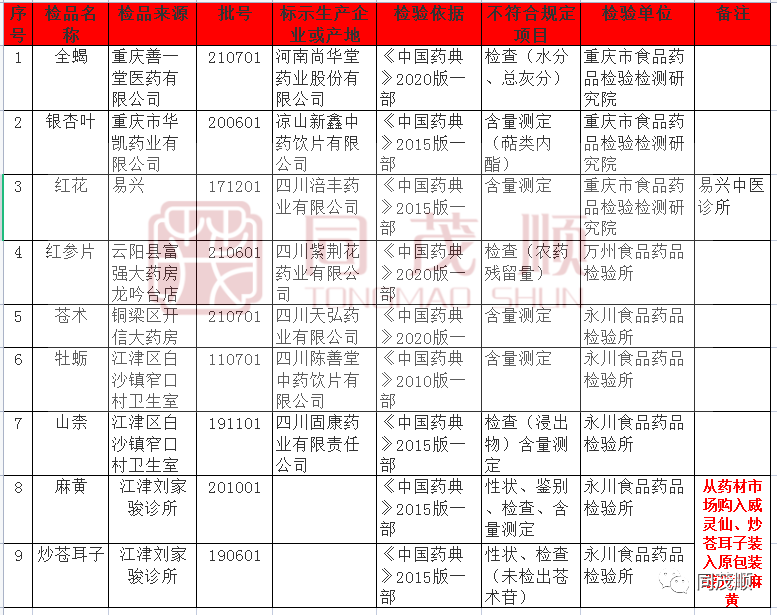
一、经重庆市食品药品检验检测研究院检验,标示为河南尚华堂药业股份有限公司生产的全蝎(批号:210701)检查(水分、总灰分)不符合规定;标示为凉山新鑫中药饮片有限公司生产的银杏叶(批号:200601)和四川涪丰药业有限公司生产的红花(批号:171201)含量测定不符合规定。
二、经重庆市万州食品药品检验所检验,标示为四川紫荆花药业有限公司生产的红参片(批号:210601)检查(农药残留量)不符合规定。
三、经重庆市永川食品药品检验所检验,标示为四川天弘药业有限公司生产的苍术(批号:210701)和四川陈善堂中药饮片有限公司生产的牡蛎(批号:110701)含量测定不符合规定;标示为四川固康药业有限责任公司生产的山柰(批号:191101)检查和含量测定不符合规定;在江津刘家俊诊所抽样的麻黄和炒苍耳子性状、检查等项目不符合规定。
对以上不符合规定的产品,重庆市药品监督管理局已责成有关直属检查局和区县药品监管部门采取查封、扣押、暂停销售、召回等必要的控制措施,依据相关法律法规进行查处。
附件:9批次不符合规定药品名单
第九十八条 禁止生产(包括配制,下同)、销售、使用假药、劣药。 有下列情形之一的,为假药:
(一)药品所含成份与国家药品标准规定的成份不符;
(二)以非药品冒充药品或者以他种药品冒充此种药品;
(三)变质的药品;
(四)药品所标明的适应症或者功能主治超出规定范围。
生产、销售劣药:第一百一十七条 生产、销售劣药的,没收违法生产、销售的药品和违法所得,并处违法生产、销售的药品货值金额十倍以上二十倍以下的罚款;违法生产、批发的药品货值金额不足十万元的,按十万元计算,违法零售的药品货值金额不足一万元的,按一万元计算;情节严重的,责令停产停业整顿直至吊销药品批准证明文件、药品生产许可证、药品经营许可证或者医疗机构制剂许可证。生产、销售的中药饮片不符合药品标准,尚不影响安全性、有效性的,责令限期改正,给予警告;可以处十万元以上五十万元以下的罚款。生产、销售假药,或者生产、销售劣药且情节严重:第一百一十八条 生产、销售假药,或者生产、销售劣药且情节严重的,对法定代表人、主要负责人、直接负责的主管人员和其他责任人员,没收违法行为发生期间自本单位所获收入,并处所获收入百分之三十以上三倍以下的罚款,终身禁止从事药品生产经营活动,并可以由公安机关处五日以上十五日以下的拘留。
来源:同茂顺







 甘公网安备 62112602000025号
甘公网安备 62112602000025号